严格的质量控制协议必须加以使用,以保证一个特定的介质能够恢复所有种类的微生物可能存在临床样本英寸,我们的目的是评估替代协议将使我们能够探测中等故障产生的病原菌选择数量上的增长,并与M22-A2从NCCLS文件进行比较。本文缔一生物/缔一生物为您分析质量控制微生物培养基,是否足以遵循NCCLS M22-A2程序?
使用S.SBA结果肺炎和S.无乳链球菌,和TM随N脑膜炎或N.淋球菌,表现出菌落计数方面没有显着性差异,不论媒体来源。
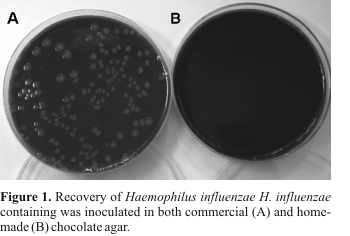
巧克力琼脂,另一方面,显示出对于H的恢复显着差流感(图1),在内部的板显示恢复此有机体相比商业板的能力有限。事实上,可以得到仅5菌落预期菌落计数为4.5×103CFU。
在CA板使用NCCLS M22-A2文档,它使用已知的是提供1至2×104CFU/板细菌悬浮液,显示出典型的菌落中描述的程序也测试,而不考虑其来源。这一结果是根据我们的试验中获得的结果,当104H的CFU流感接种在商业和内部巧克力琼脂平板,如果只生长或非生长将被记录下来。
在NCCLS M22-A2文档中描述的过程可用于检查失败,以支持生长或产率的预期菌落大小。我们内部的媒体都被批准后的M22-A2的指导方针。然而,我们的结果表明,一些媒体可能必须恢复苛养微生物,如H的能力有限流感,也就是按照与先前公布的数据(1)。
总之,我们在这里报告的一些媒体的生长能力的变异性,特别是分离考究生物体像H.流感。检查所有媒体具有两个或多个生物体的几个稀释度可能是不必要的。我们建议,只有那些用于恢复挑剔病原体,可能存在在一个关键的临床样品中的浓度非常低,媒体使用这里描述的协议进行测试。对其它不太关键媒体,继NCCLS M22-A2准则可以是足够的。
综上所述,您是不是已经对质量控制微生物培养基,是否足以遵循NCCLS M22-A2程序,有所了解。如果还有其他疑问,请咨询缔一生物/缔一生物资深专家。